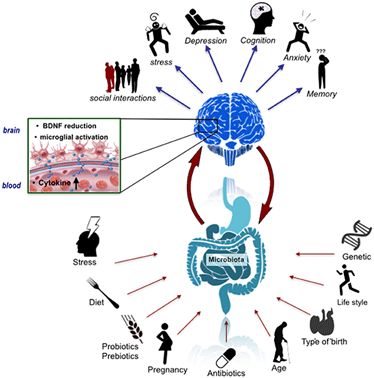
유전자는 자폐증의 강력한 추동요인일 수 있다. 그러나 어떤 연구자들은 또 다른 요인이 작용할 수 있다고 생각하고 있다. 그것은 바로 장내미생물(gut bacteria), 즉 소화관에 서식하는 미생물군(群)이다. 이 생각은 논란이 많았지만, 새로운 연구에서 이 같은 「장(腸)-뇌 관련성(gut-brain link)」을 뒷받침하는 결과가 나왔다. 구체적으로, "생쥐에게 자폐증 환자의 대변에서 채취한 세균을 투입해보니, 자폐유사행동(autismlike behavior)이 발달하더라"는 것이다. 이번 연구결과가 "장내미생물이 자폐증을 초래한다"고 증명한 것은 아니지만, "최소한 생쥐의 경우, 장내미생물의 구성이 자폐증의 전형적인 증상 중 일부에 기여할 수 있다"는 것을 시사한다.
"이건 매우 고무적인 논문이다"라고 아일랜드 유니버시티 칼리지 코크의 존 크라이언(신경과학)은 논평했다. "대사물(metabolite: 세균의 소화에서 생성되는 분자)이 뇌의 활동에 영향을 미칠 수 있다는 생각은 설득력이 높으며, 마이크로바이옴 분야의 발달에 기여할 것이다."
많은 연구자들은 "자폐증 환자와 그렇지 않은 사람은 장내미생물 구성이 다르다"는 점을 발견했다. 그러나 그들이 "미생물 불균형(microbial imbalance)이 자폐증상에 기여한다"거나, "미생물불균형이 자폐증의 결과다"라고 단정한 것은 아니다.
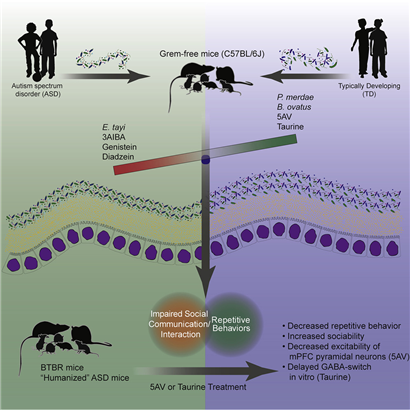
「장내미생물이 행동에 미치는 영향」을 검증하기 위해, 칼텍의 사키스 매즈매니언(미생물학)과 동료들은 '자폐아'와 '그렇지 않은 어린이'의 대변샘플을 무균생쥐(germ-free mice: 자기 자신의 마이크로바이옴을 보유하지 않은 생쥐)의 위(胃)에 투여했다. 그런 다음 동일한 마이크로바이옴을 보유한 생쥐쌍을 교배하여, 그들의 새끼가 생애초기에 인간미생물군에 노출되도록 했다.
마지막으로, 연구진은 새끼생쥐들을 대상으로, 생쥐의 자폐유사증상을 측정하는 전형적인 행동테스트를 실시했다. 즉, 그들은 생쥐가 '소리를 내는 빈도'와 '다른 생쥐에게 접근하여 상호작용을 하는 빈도'를 측정했다. 또한 케이지 안에 구슬을 뿌려놓고 몰두하는 생쥐들의 수를 헤아림으로써, 일부 자폐증 환자들에게서 볼 수 있는 반복행동(repetitive behavior)을 측정하려고 노력했다. 그 결과, '자폐아의 마이크로바이옴을 이식받은 생쥐'는 '자폐증이 없는 어린이'의 장내미생물을 이식받은 생쥐에 비해, 사회성이 낮고(less social) 더 반복적인 행동(more repetitive behavior)을 보이는 것으로 나타났다. 그들은 이상의 연구결과를 5월 30일 《Cell》에 발표했다(참고 1).
자폐증 환자에게서 유래한 마이크로바이옴에는 다수의 유익균(beneficial bacteria: 연구자들이 유익하다고 생각하는 미생물종) 수준이 낮은 것으로 나타났다. 장내미생물은 식품 속의 아미노산을 분해하거나 변형하며, 그 부산물이 혈류를 타고 뇌로 유입될 수 있는 것으로 알려져 있다(참고 2). 그러나 정확히 어떤 미생물이 뇌와 상호작용을 통해 자폐유사증상에 영향을 미치는지는 알려져 있지 않다.
연구진이 생쥐의 뇌를 절개하여 RNA 분석을 해본 결과, 두 생쥐그룹은 560개 유전자에 대한 스플라이싱(splicing: DNA 메시지가 단백질로 번역되기 전에 처리되는 방법)이 다른 것으로 밝혀졌다. "560개 중 52개는 자폐증과 관련된 것으로 알려진 유전자인데, 이것은 흥미로운 시사점을 제공한다. 즉, 장내미생물의 생성물이 '뇌에서 만들어지는 단백질의 형태'에 영향을 미침으로써, 자폐위험을 변화시킨다는 것이다"라고 이번 연구의 제1저자인 칼텍의 길 샤론(생물학, 박사후 연구원)은 말했다.
연구진이 생쥐의 소화관 내용물을 분석한 결과, 두 그룹의 생쥐들은 27개 대사물의 수준이 다른 것으로 나타났다. 특히, 자폐아의 장내미생물을 보유한 생쥐들은 타우린(taurine)과 5-아미노발레르산(5AV: 5-aminovaleric acid)의 수준이 낮은 것으로 밝혀졌는데, 이 분자들은 뉴런에 결합하여 활성을 억제하는 것으로 알려져 있다. 이 발견은 '흥분신호(excitatory signal)와 억제신호(inhibitory signal)의 불균형이 자폐증의 원인'이라는 이론과 부합한다. 또한 연구진이 '자폐유사증상이 나타나는 것으로 알려진 생쥐계열'에게 타우린이나 5AV를 먹여본 결과, 사회적 상호작용이 증가하고 반복행동이 줄어든 것으로 나타났다.
"누락된 연결고리가 아직도 많다"라고 하버드 대학교에서 세균과 뇌기능 간의 관계를 연구하는 허준렬 교수(면역학; 참고 3)는 논평했다. "그러나 이번 연구의 진정한 중요성은 「미생물군과 자폐유사행동 간의 인과관계」를 사상 최초로 입증한 데 있는 것으로 사료된다."
"다음 과제는, 미국인 말고 다른 나라 사람들의 대변샘플을 이용하여 이번 연구결과를 재현하는 것이다. 인간의 상주미생물(resident microbe)은 환경과 식생활에 기반하므로, 미국인의 마이크로바이옴 차이가 자폐위험에 영향을 미치는지 여부는 아직 미스터라라고 할 수 있다"라고 호주 스윈번 공과대학에서 장내미생물을 연구하는 샤쿤틀라 곤달리아는 말했다.
"이번 연구결과가 당장 새로운 마이크로바이옴기반 치료법(microbiome-based treatment)으로 이어질 가능성은 낮다. 왜냐하면, 이번 연구에서 강조된 두 개의 대사물은 사람의 자폐증과 무관한 것으로 밝혀질 수도 있기 때문이다"라고 크라이언은 말했다. 그럼에도 불구하고, 연구진은 이번 연구에서 '자폐증 환자의 장(腸)이나 뇌(腦)에 결핍된 다른 대사물을 찾아야 한다'는 명분을 제시했다. "이번 연구는 마이크로바이옴 학계에 '거기에 뭔가가 있다(there is something there)'는 긍정적 시그널을 보냈다"라고 그는 덧붙였다.
이번 연구의 하이라이트
1. 인간의 ASD 마이크로바이옴을 보유한 생쥐는 ASD 유사행동을 보이지만, TD 마이크로바이옴을 보유한 생쥐는 그렇지 않다.
2. ASD 마이크로바이옴과 TD 마이크로바이옴은, 생쥐에서 상이한 대사체 프로파일(metabolome profile)을 나타냈다.
3. ASD 마이크로바이옴을 보유한 생쥐의 뇌에서, 위험유전자의 광범위한 대체 스플라이싱(alternative splicing)이 관찰되었다.
4. 타우린이나 5AV로 치료된 BTBR 생쥐는 반복행동과 사회적 행동이 향상되었다.
※ 참고문헌
1. http://doi.org//10.1016/j.cell.2019.05.004
2. http://www.ibric.org/myboard/read.php?Board=news&id=297953&SOURCE=6
3. https://huhlab.med.harvard.edu/
※ 출처: Science http://www.sciencemag.org/news/2019/05/gut-bacteria-may-contribute-autism-symptoms-mouse-study-finds
글쓴이_양병찬
서울대학교 경영학과와 동 대학원을 졸업한 후 기업에서 근무하다 진로를 바꿔 중앙대 학교에서 약학을 공부했다. 약사로 일하며 틈틈이 의약학과 생명과학 분야의 글을 번역했다. 포항공과대학교 생물학연구정보센터BRIC의 바이오통신원으로, <네이처>와 <사이언스>등에 실리는 의학 및 생명과학 기사를 실시간으로 번역, 소개하고 있다. 그의 페이스북에 가면 매일 아침 최신 과학기사를 접할 수 있다.
https://www.facebook.com/OccucySesamelStreet


서로 반대되는 내용과 설명의 글을 <양병찬> 한 분이 올리셨는데......
어떻게 된 사연일까요?